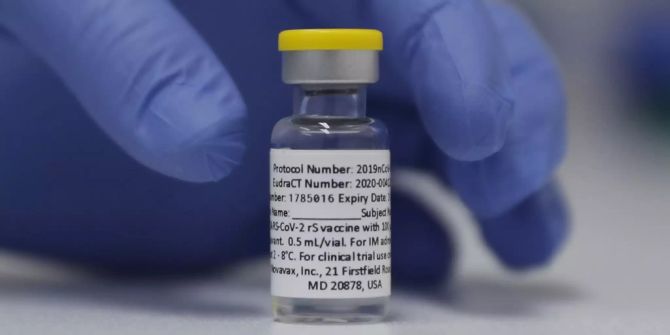
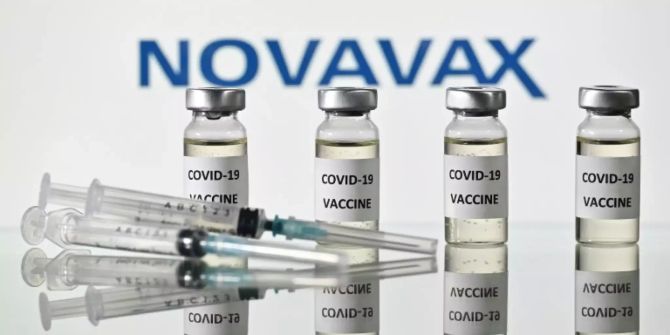
Novavax plant Zulassungsantrag für Impfstoff in Q3
Novavax erzielte weitere positive Studienergebnisse für sein Vakzin. Darum stellt das Biotechunternehmen einen Antrag für eine Zulassung im dritten Quartal.
Das Wichtigste in Kürze
- Das Vakzin von Novavax hat laut ihrer neuen Studie eine Wirksamkeit von 93 Prozent.
- Deshalb will das Biotechunternehmen eine Zulassung für das dritte Quartal beantragen.
Das US-Biotechunternehmen Novavax plant nach weiteren positiven Studienergebnissen mit seinem Covid-19-Impfstoff nun einen Zulassungsantrag im dritten Quartal.
In einer Studie mit rund 30'000 Teilnehmern in den USA und Mexiko zeigte das Vakzin eine Wirksamkeit von 93 Prozent. Dies gegen alle vorherrschenden Virusvarianten, wie Novavax am Montag mitteilte.
Während der Untersuchung sei die erstmals in Grossbritannien aufgetretene Alpha-Variante B.1.1.7 am häufigsten aufgetreten. Studienteilnehmer hätten sich aber auch mit den Varianten aus Brasilien, Südafrika und Indien infiziert, sagte Novavax-Forschungschef Gregory Glenn.
Der Impfstoff schützte Studienteilnehmer, die ein hohes Risiko für einen schweren Verlauf hatten, demnach zu 91 Prozent. Und zeigte eine Wirksamkeit von 100 Prozent bei der Vorbeugung mittelschwerer und schwerer Covid-19-Fälle. Gegen Varianten, die Novavax nicht identifizieren konnte, sei er zu etwa 70 Prozent wirksam gewesen, sagte Glenn.
Produktionsziele mussten verschoben werden
Novavax hatte bereits zu Jahresbeginn erste Daten aus seiner Studie in Grossbritannien vorgelegt. Wonach das Vakzin eine Wirksamkeit von gut 89 Prozent zeigte. Das Unternehmen hatte aber mehrmals seine Produktionsziele verschieben müssen.
Und kämpfte mit Engpässen bei Materialien und Zubehör zur Herstellung seines Impfstoffs. Bis Ende des dritten Quartals will der Konzern 100 Millionen Impfdosen pro Monat herstellen. Und 150 Millionen Dosen monatlich bis Ende des vierten Quartals.