EU-Arzneimittelbehörde prüft bedingte Zulassung von Remdesivir gegen Covid-19
Die EU-Arzneimittelbehörde EMA prüft derzeit eine bedingte Marktzulassung des Medikaments Remdesivir für Corona-Patienten.
Das Wichtigste in Kürze
- Behörde verspricht beschleunigtes Prüfverfahren.
Ihr liege eine Anfrage für die bedingte Marktzulassung des antiviralen Medikaments zur Behandlung von Covid-19 vor, teilte die Behörde am Montag mit. Eine Prüfung sei eingeleitet worden.
Die EMA kündigte zugleich an, das Prüfverfahren hinsichtlich der Vorteile und der Risiken zu beschleunigen. Eine Einschätzung könne bereits in «einigen Wochen» vorliegen.
Die US-Arzneimittelbehörde FDA hatte Anfang Mai eine Notfall-Genehmigung für den Einsatz des Wirkstoffs in Krankenhäusern erteilt. Japan zog kurze Zeit später nach, Europa plant eine ähnliche Entscheidung.
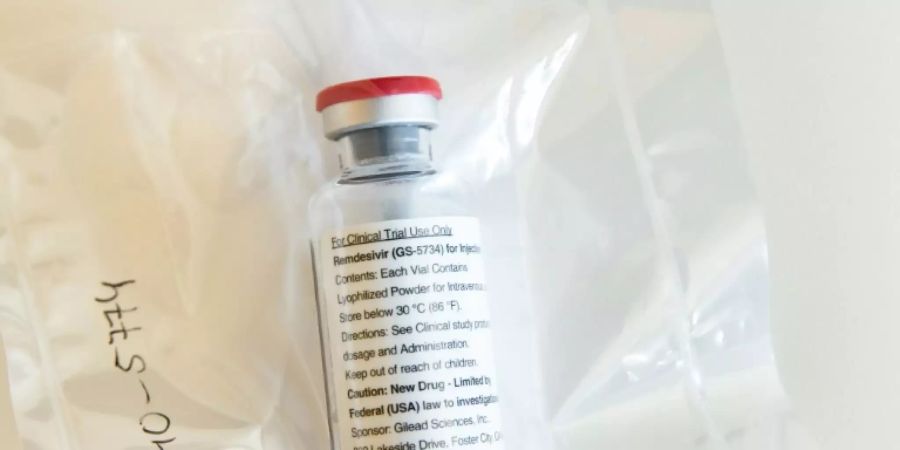
Das vom US-Hersteller Gilead produzierte Remdesivir wurde eigentlich zur Behandlung von Ebola entwickelt. Bei der Behandlung von Covid-19-Patienten ist es bislang das einzige Medikament, das in klinischen Tests eine gewisse Wirksamkeit zeigte. Dennoch gilt der Erfolg als moderat.














