Blutplasma zur Behandlung von Covid-19-Patienten in den USA generell zugelassen
Die US-Behörden haben den Einsatz von Blutplasma bei der Behandlung von Erkrankungen an dem neuartigen Coronavirus generell erlaubt.
Das Wichtigste in Kürze
- Wirksamkeit in der Fachwelt aber weiterhin umstritten.
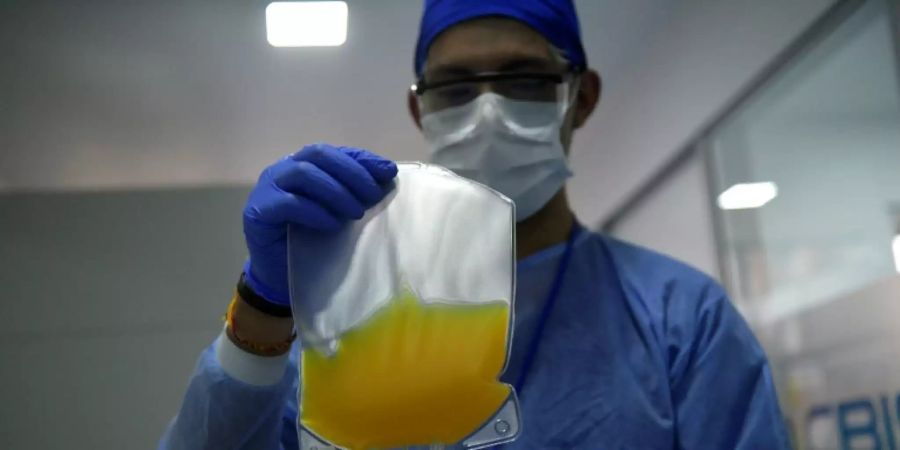
Das Plasma könne bei der Therapie der von dem Erreger ausgelösten Lungenkrankheit Covid-19 «effektiv» sein, erklärte am Sonntag die Arzneimittelaufsichtsbehörde FDA. Das Plasma stammt von genesenen Covid-19-Patienten und enthält Antikörper gegen das Virus.
Die Zulassung des Plasmas für die Behandlung von Covid-19-Patienten war auf Grundlage einer Sondergenehmigung für Notstandssituationen beschleunigt worden. US-Präsident Donald Trump sagte am Sonntag bei einer Pressekonferenz im Weissen Haus, die Plasma-Therapie zeige eine «unglaubliche Erfolgsrate» und werde «zahllose Leben retten».
Trump äusserte sich damit allerdings deutlich euphorischer als die FDA, die lediglich von einem «potenziellen Nutzen» des Plasmas sprach, der grösser sei als die bekannten Nebenwirkungen.
Das Blutplasma von genesenen Covid-19-Erkrankten wurde bereits in den USA eingesetzt, allerdings nur unter starken Einschränkungen. Erlaubt war die Transfusion des Plasmas bislang nur im Rahmen von klinischen Tests und bei Patienten in besonders schlechtem Zustand. Durch die jetzt von der FDA erteilte Genehmigung ist die generelle Anwendung von Plasma bei der Behandlung von Covid-19-Patienten möglich.
Nach Angaben von US-Gesundheitsminister Alex Azar hatten die bislang mit Plasma behandelten Covid-19-Kranken in den USA eine um 35 Prozent höhere Überlebensrate als andere Patienten mit der gleichen Krankheit. Wie effektiv der Einsatz von Plasma im Kampf gegen das Coronavirus tatsächlich ist, ist in der Fachwelt allerdings umstritten. Manche Experten warnen vor starken Nebenwirkungen.










