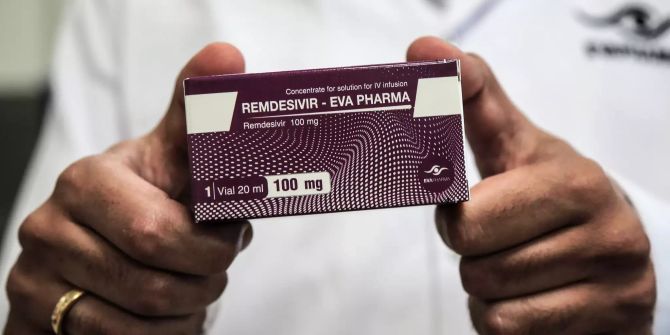
Erste europäische Zulassung für ein Corona-Arzneimittel
Als erstes Corona-Mittel hat Remdesivir die Zulassung in Europa erhalten. Das hat die EU-Kommission im Schnellverfahren entschieden.

Das Wichtigste in Kürze
- Bisher fehlen in Europa ein Impfstoff, sowie ein zugelassenes Medikament gegen Corona.
- Nun hat die EU-Kommission dem Wirkstoff Remdesivir die Zulassung erteilt.
- Sie hat einen entsprechenden Antrag im Schnellverfahren behandelt.
Bislang gibt es gegen das Coronavirus keinen Impfstoff und kein zugelassenes Medikament. Nun hat die EU-Kommission einem vielversprechenden Wirkstoff unter Auflagen die Zulassung für den europäischen Markt erteilt.
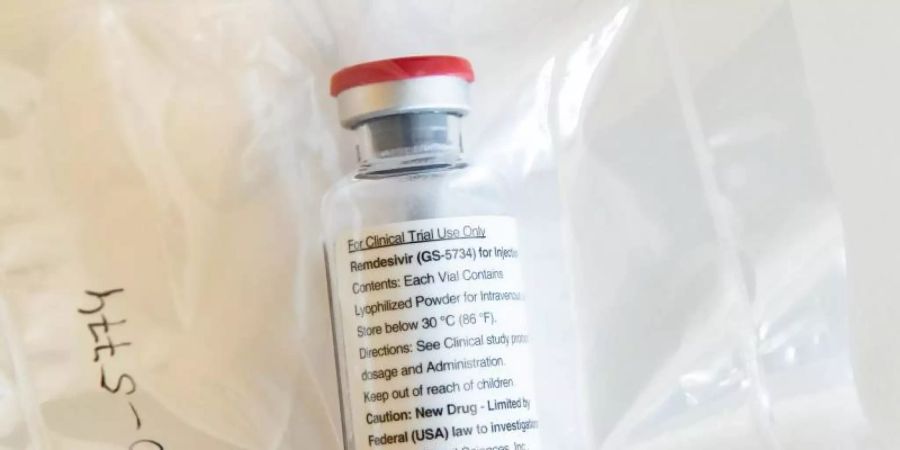
Der Wirkstoff Remdesivir wird in Europa unter Auflagen als erstes Mittel zur Therapie von Covid-19 zugelassen. Die Entscheidung gab die EU-Kommission bekannt.
Gesundheitskommissarin Stella Kyriakides erklärte: «Die heutige Zulassung eines ersten Medikaments zur Behandlung von Covid-19 ist ein wichtiger Fortschritt im Kampf gegen das Virus.» Die Zulassung sei im Schnellverfahren weniger als einen Monat nach dem Antrag ergangen.
Kein Allheilmittel, aber ein Lichtblick
Remdesivir gilt als eine von wenigen wirksamen Arzneien bei schweren Fällen der vom Coronavirus ausgelösten Lungenkrankheit. Es kann Studien zufolge den Krankenhausaufenthalt verkürzen. Die Europäische Arzneimittel-Agentur EMA hatte die Zulassung für Patienten ab zwölf Jahren empfohlen. Dies, wenn sie eine Lungenentzündung haben und mit zusätzlichem Sauerstoff versorgt werden müssen.
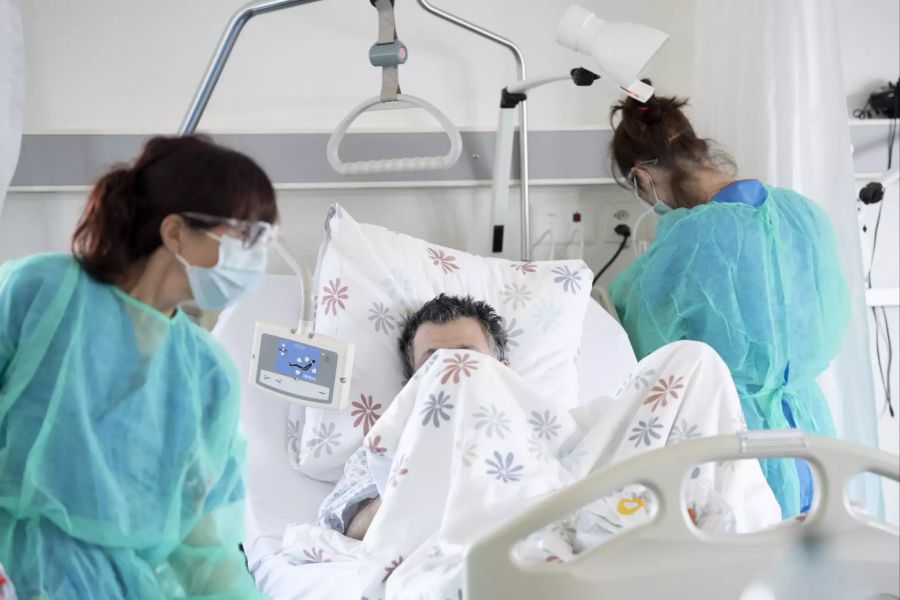
Ärzte sehen Remdesivir nicht als Allheilmittel, wohl aber als Lichtblick für Corona-Patienten. Eine internationale Studie mit über 1000 Teilnehmern hatte Ende April gezeigt: Remdesivir kann bei Covid-19-Patienten die Zeit bis zu einer Genesung im Schnitt um vier Tage verkürzen. Von 15 auf 11 Tage.
Die USA hatten bereits Anfang Mai eine Ausnahmegenehmigung für den begrenzten Einsatz des Wirkstoffes in Krankenhäusern erteilt. Auch in Deutschland war das Mittel bislang schon innerhalb eines Arzneimittel-Härtefallprogrammes zugänglich und wurde in klinischen Studien getestet.
USA kauft gesamte Produktionsmenge auf
Die US-Regierung hatte diese Woche eine Vereinbarung mit dem US-Hersteller Gilead Sciences bekannt gemacht. Demnach hat sie praktisch die gesamte Produktionsmenge des Mittels für die nächsten Monate aufgekauft. Allerdings hat zum Beispiel Deutschland bereits Vorräte angelegt. Die EU-Kommission verhandelt ebenfalls mit dem Hersteller, um sich ausreichende Mengen des Wirkstoffs zu sichern.

Der CDU-Europapolitiker Peter Liese betonte, Bedingung für die Zulassung in Europa sei, dass der Hersteller auch nach Europa liefere. Eine mögliche Lösung für Engpässe wäre, dass Gilead seine Kenntnisse mit anderen Herstellern teile und diese gegen Lizenzgebühren produzieren lasse. Auch damit könne Gilead sehr viel Geld verdienen, sagte Liese.
Remdesivir wurde ursprünglich zur Behandlung von Ebola entwickelt, zeigte aber eine zu geringe Wirkung. Es ist bislang in keinem Land der Welt uneingeschränkt als Medikament zugelassen. Bislang gibt es keine Impfung gegen das neuartige Coronavirus und auch keine zuverlässige zugelassene medikamentöse Therapie.